1. NGS 임상검사실의 품질관리체계, 숙련도 및 검사성능 등의 인증에 대한 검토는 식약처에서 시행한다.
2. 식품의약품안전처장은「체외진단의료기기법」제12조7항에 따라 같은 조제2항에 따른 임상검사실의 품질관리체계 및 숙련도 평가 업무를 식품의약품안전처장이 정하여 고시하는 기관 또는 단체에 위탁이 가능하다.
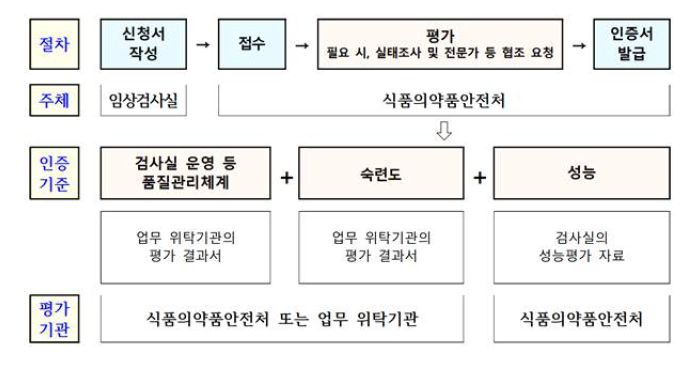
3. NGS 임상검사실에 대한 평가는 NGS 임상검사실에 대한 품질관리 체계 및 숙련도평가와 해당 검사실에서 수행하는 NGS 검사에 대한 성능평가로 이루어진다.
4. NGS 임상검사실의 NGS 검사 인증의 유효기간은 인증을 받은 날부터 3년으로 하며, 인증의 갱신을 위해서는 인증의 유효기간이
끝나기 3개월 전에 인증을 신청할 수 있다.
5. 변경인증을 받으려는 경우에는 그 변경사유가 발생한 날부터 30일 이내에「체외진단의료기기법」시행규칙 별지 제21호 서식의 임상 검사실의 체외진단검사 변경인증신청서(전자문서 포함)를 첨부하여 식품의약품안전처장에게 제출한다.
1. 준수사항
가. 인증을 받은 NGS 임상검사실은 다음의 사항을 준수해야 한다.
- NGS 검사의 전년도 실적을 매년 1월 31일까지 식품의약품안전처장에게 제출할 것
- NGS 검사와 관련된 문서 및 기록을 해당 검사가 끝난 날부터 3년 동안 보관할 것
- NGS 검사의 실시 중 중대한 이상사례가 발생한 경우에는 식품의약품안전처장에게 보고할 것
- NGS 임상검사실은 NGS 검사에 대해 인증기준을 유지할 것
나. NGS 임상검사실은 「생명윤리 및 안전에 관한 법률」에 따라 유전자검사기관으로서의 업무정지 등 명령을 받은 경우에는 해당
사실을 즉시 식품의약품안전처장에게 보고하여야 한다.
2. 자문
가. 식품의약품안전처장은 체외진단의료기기 허가 및 안전관리에 관한 사항을 조사ㆍ심의하기 위하여
식품의약품안전처에 체외진단의료기기 전문가위원회를 두어 자문을 받을 수 있다.
'차세대염기서열분석(NGS) 임상검사실 인증' 카테고리의 다른 글
| 차세대염기서열분석(NGS) 임상검사실인증 평가 분야 및 기준 (5) 신청 및 평가 (0) | 2025.12.26 |
|---|---|
| 차세대염기서열분석(NGS) 임상검사실인증 평가 분야 및 기준 (4) 인증 기준 (0) | 2025.12.26 |
| 차세대염기서열분석(NGS) 임상검사실인증 평가 분야 및 기준 (3) 검사성능 (0) | 2025.12.26 |
| 차세대염기서열분석(NGS) 임상검사실인증 평가 분야 및 기준 (2) 숙련도 (0) | 2025.12.26 |
| 차세대염기서열분석(NGS) 임상검사실인증 평가 분야 및 기준 (1) 품질관리체계 (0) | 2025.12.26 |



