▶ 기술문서와 함께 추가적으로 내야하는 자료의 종류로는 아래와 같다.
1. 제품 정보 관련정보
1) 기 허가 제품과 비교한 자료
2) 사용목적에 관한 자료
3) 작용원리에 관한 자료
4) 기원 또는 발견 및 개발경위에 관한 자료
5) 외국의 사용현황 등에 관한 자료
2. 제품의 안전성 및 유효성(성능) 검증에 필요한 자료
1) 안전성 : 신뢰성이 확보된 시험기관이 해당 제품의 안전을 확인하기 위해 시험한 실측치 자료
- 전기·기계적 안전에 관한 자료
- 생물학적 안전에 관한 자료
- 방사선에 관한 안전성 자료
- 전자파안전에 관한 자료
2) 성능 : 제조자가 의도한 사용목적이 달성되도록 하기 위한 물리적·기계적 기능을 확인하기 위하여 시험한 실측치 자료
- 물리·화학적 특성에 관한 자료
- 성능에 관한 자료
3) 제품의 사용기간(유효기간)을 검증을 위한 자료
- 안정성에 관한 자료
4) 임상시험에 관한 자료
▶ 정리를 해보면 이렇게 나열할 수 있다.
기술문서 첨부자료 종류
1. 제품 정보 관련정보
2. 제품의 안전성 및 유효성 ( 성능 ) 검증에 필요한 자료
1) 기허가 제품과
비교한 자료
1) 안전성
2) 성능
3) 제품의 사용기간
( 유효기간 ) 을 검증을 위한 자료
4) 임상시험에
관한 자료
2) 사용목적에
관한 자료
전기 · 기계적 안전에 관한 자료
물리 · 화학적 특성에
관한 자료
안정성에 관한 자료
3) 작용원리에
관한 자료
생물학적 안전에 관한 자료
4) 기원 또는 발견 및 개발경위에 관한 자료
방사선에 관한 안전성 자료
성능에 관한 자료
5) 외국의 사용현황 등에 관한 자료
전자파안전에 관한 자료
▶ 하지만 제품마다 품목마다 이 자료들을 다 내야하는 걸까?
그렇다면 제품마다 품목마다 어떤자료를 내야하는지 가늠하기 어렵다면
법제처 의료기기 검색후 행정규칙 클릭 의료기기 허가 신고 심사등에 관한 규정
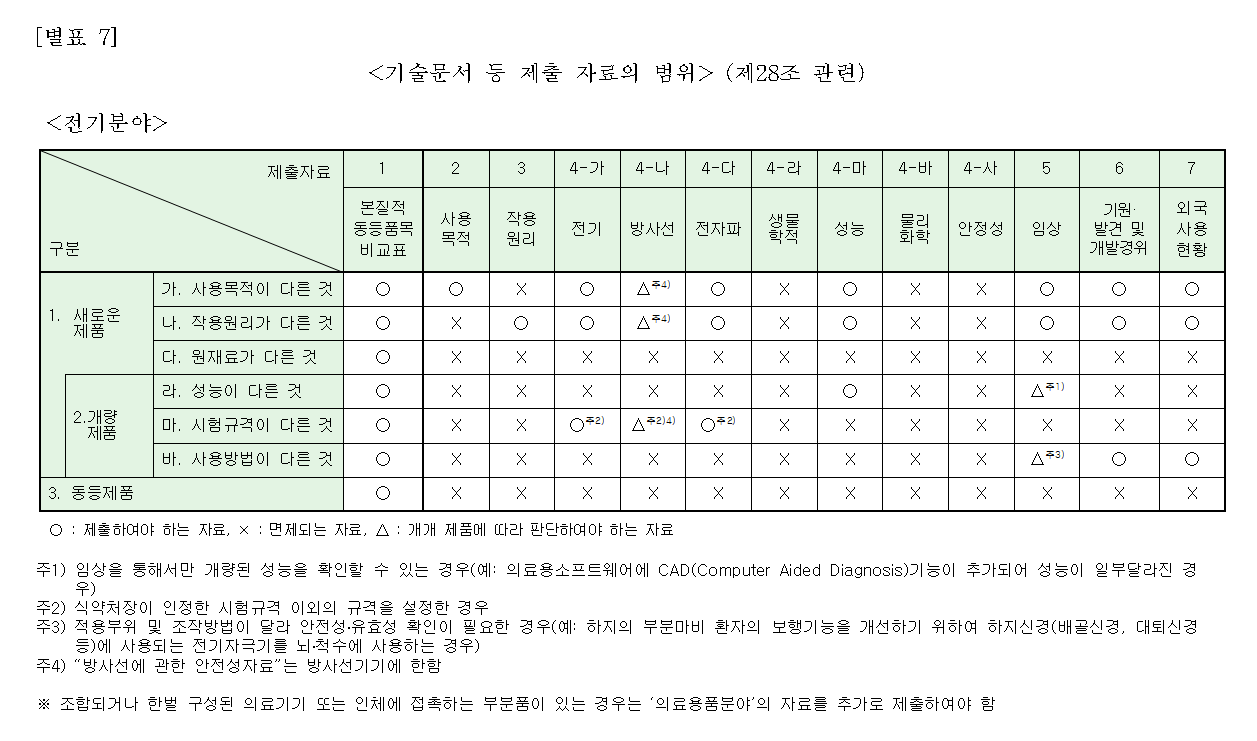
[별표 7] 기술문서 등 제출자료의 범위를 확인하자!
[ 별표 7] < 기술문서 등 제출 자료의 범위 > ( 제 28 조 관련 )
[별표 7] 기술문서 등 제출 자료의 범위(제28조 관련).hwp
0.70MB
▶ 파일을 확인하면 전기분야, 의료용품 두가지 및 중분류별로 나뉘어져있다.
전기 의료기기 기술문서 첨부자료 제출범위
의료용품 기술문서 첨부자료 제출범위
전기를 사용하는 의료기기와 용품은 대략적으로는 이렇고 파일 아래로 내려보면
품목별로도 있다.
중분류별 기술문서 자료 제출범위 (105 개 )가 있으니 해당되는 중분류가 어딘지 확인해보자!
중분류를 모르겠으면 아래 링크참고!
만약 품목별로 나와있는 자료 범위에서 △가 있거나 잘 모르겠으면
의료기기안전정보원이나 식약처쪽 담당자에게 전화해서 물어보자!
의료기기 안전정보원은 홈페이지 조직도 부분에 인증본부에 연락해서 품목말하고 담당자 연결 부탁하거나
http://www.nids.or.kr/contents.jsp?page=NIDS-080
한국의료기기안전정보원에 오신 걸 환영합니다
정책연구실 실장 이상우 · 정책연구실 총괄 02-860-4341 정책연구팀 팀장 여창민 · 의료기기 규제영향 분석 및 규제 거버넌스 발전전략 연구 · 의료기기 정책연구 및 정책개발 수행 · 위탁사업 수행 및 총괄 관리 02-860-4342 팀원 이효석 · 국내외 의료기기 규제정책 현황 및 정책연구 ‧분석 · 위탁용역(통합정보뱅크) 사업계획, 실적, 연구행정(사업비 등) 관리 · 위탁용역(통합정보뱅크) 인허가단계 콘텐츠 정보 수집·분석 02-860-4343
www.nids.or.kr
1577-1255 식약처 상담전화!
4번 의료기기 누르고 상담원에게 품목 말하고
허가 담당자 부서, 번호와 이름좀 알려달라고 하자!
★ 미리 첨부자료 파악하고 제출해야지 미리 준비가 가능하다!
https://toucrew.tistory.com/65?category=853558
의료기기 품목 및 품목별 등급에 관한 규정
의료기기 품목 및 품목별 등급에 관한 규정 [별표 1] 의료기기의 등급분류 및 지정에 관한 기준과 절차(제2조 관련) 등급의 지정절차 식품의약품안전처장은 의료기기를 다음 각 목의 구분에 따라 대분류, 중분류,..
toucrew.tistory.com
범용전기수술기 기술문서 첨부자료 범위
<전기분야>
제출자료
구분
1
2
3
4- 가
4- 나
4- 다
4- 라
4- 마
4- 바
4- 사
5
6
7
본질적 동등품목
비교표
사용
목적
작용
원리
전기
방사선
전자파
생물 학적
성능
물리
화학
안정성
임상
기원 ∙
발견 및 개발경위
외국 사용 현황
1.
새로운
제품
가 . 사용목적이 다른 것
○
○
X
○
△ 주 4)
○
X
○
X
X
○
○
○
나 . 작용원리가 다른 것
○
X
○
○
△ 주 4)
○
X
○
X
X
○
○
○
다 . 원재료가 다른 것
○
X
X
X
X
X
X
X
X
X
X
X
X
2. 개량
제품
라 . 성능이 다른 것
○
X
X
X
X
X
X
○
X
X
△ 주 1)
X
X
마 . 시험규격이 다른 것
○
X
X
○ 주 2)
△ 주 2)4)
○ 주 2)
X
X
X
X
X
X
X
바 . 사용방법이 다른 것
○
X
X
X
X
X
X
X
X
X
△ 주 3)
○
○
3. 동등제품
○
X
X
X
X
X
X
X
X
X
X
X
X
○ : 제출하여야 하는 자료, × : 면제되는 자료, △ : 개개 제품에 따라 판단하여야 하는 자료
주1) 임상을 통해서만 개량된 성능을 확인할 수 있는 경우(예: 의료용소프트웨어에 CAD(Computer Aided Diagnosis)기능이 추가되어 성능이 일부달라진 경우)
주2) 식약처장이 인정한 시험규격 이외의 규격을 설정한 경우
주3) 적용부위 및 조작방법이 달라 안전성․유효성 확인이 필요한 경우(예: 하지의 부분마비 환자의 보행기능을 개선하기 위하여 하지신경(배골신경, 대퇴신경 등)에 사용되는 전기자극기를 뇌․척수에 사용하는 경우)
주4) “방사선에 관한 안전성자료”는 방사선기기에 한함
※ 조합되거나 한벌 구성된 의료기기 또는 인체에 접촉하는 부분품이 있는 경우는 ‘의료용품분야’의 자료를 추가로 제출하여야 함
<의료용품분야>
제출자료
구분
1
2
3
4- 가
4- 나
4- 다
4- 라
4- 마
4- 바
4- 사
5
6
7
본질적 동등품목
비교표
사용
목적
작용
원리
전기
방사선
전자파
생물 학적
성능
물리
화학
안정성
임상
기원 ∙
발견 및 개발경위
외국 사용 현황
1.
새로운
제품
가 . 사용목적이 다른 것
○
○
X
X
X
X
○
○
○
○
○
○
○
나 . 작용원리가 다른 것
○
X
○
X
X
X
○
○
○
○
X
○
○
다 . 원재료가 다른 것
○
X
X
X
X
X
○
○
○
○
△ 주 1)
○
○
2. 개량
제품
라 . 성능이 다른 것
○
X
X
X
X
X
X
○
X
X
X
X
X
마 . 시험규격이 다른 것
○
X
X
X
X
X
○
X
X
X
X
X
X
바 . 사용방법이 다른 것
○
X
X
X
X
X
X
X
X
X
△ 주 2)
○
○
3. 동등제품
○
X
X
X
X
X
X
X
X
X
X
X
X
○ : 제출하여야 하는 자료, × : 면제되는 자료, △ : 개개 제품에 따라 판단하여야 하는 자료
주1) 기 허가·인증된 제품에서 한번도 사용되지 않은 원재료를 사용하는 경우(예: 치과재료에 새로운 고분자 또는 금속을 적용하는 경우)
주2) 적용방법이 달라 안전성․유효성 확인이 필요한 경우(예: 개방되지 않은 창상에 적용하여 흉터를 최소화하는데 사용하는 점착성투명창상피복재를 개방된 창상에 사용하는 경우)
※ 조합되거나 한벌 구성된 의료기기 또는 전기를 사용하는 제품의 경우는 ‘전기분야’의 자료를 추가로 제출하여야 함
출처: 법제처